Die Arbeit innerhalb des KINBIOTICS-Projekts teilt sich in folgende Pakete auf:
Das Ziel dieses Arbeitspaketes ist die Entwicklung eines neuartigen Systems für die Identifizierung von Infektionserregern und ihren Antibiotika-Resistenzen mit Potential für die Anwendung im klinischen Labor.
Das System beruht auf einer Sequenziermethode der „Dritten Generation“ (Nanoporen-Sequenzierung), mit deren Hilfe DNA sehr viel schneller und kostengünstiger sequenziert werden kann. Das System ist außerdem weitgehend skalierbar und präziser als andere Identifizierungssysteme für Mikroorganismen. Insbesondere können so identische Keime bestimmt und Infektionsketten erkannt werden. Die Methodik, die im Universitätslabor bereits grundsätzlich nachgewiesen wurde, soll im Rahmen des Projektes so weiterentwickelt werden, dass sie im klinischen Alltag eingesetzt werden kann.
Weiterhin sollen Datenanalyse-Strategien entwickelt werden, mit denen sich die Wirkung der in den Genomen gefundenen Antibiotikaresistenz-Gene (MHK: minimale Hemmkonzentration) vorhersagen lassen. Diese Vorhersagen sollen durch den Abgleich mit bereits existierenden klinisch-mikrobiologischen Test-Systemen intensiv validiert werden.
Im klinischen Alltag gibt es etablierte Arbeitsschritte zur Identifizierung von pathogenen Bakterien und Charakterisierung der klinisch relevanten Antibiotikaresistenzen. Hierzu werden die den Patient*innen entnommenen Proben zunächst kultiviert. Im Fall einer Blutprobe ist das die Blutkultur, die durch Kohlendioxidbildung das Wachstum von Bakterien anzeigt. Eine Blutkultur beansprucht zumeist zwischen einem und mehreren Tagen. Anschließend werden weitere Kultivierungsschritte unternommen (Agarplattenkultur), um danach eine visuelle Identifizierung des Erregers vorzunehmen. Auch dieser Schritt dauert zwischen einem und mehreren Tagen.
Eine weitgehend automatisierte Erregeridentifizierung, die vor allem in größeren Laboren eingesetzt wird, ist an dieser Stelle die MALDI-Massenspektrometrie. Nach der Identifizierung der Erregerspezies folgt die Bestimmung der minimalen Hemmkonzentration (MHK) für eine Reihe klinisch relevanter Antibiotika. Dies wird zumeist von Laborgeräten automatisiert erledigt, benötigt aber wiederum mehrere Stunden für die Analyse.
Im KINBIOTICS-Projekt wollen wir diese Arbeitsabläufe stark verkürzen und die Sequenzdaten der Erreger nutzen, um möglichst auch die MHKs für die klinisch genutzten Antibiotika vorhersagen zu können.
Dieses Arbeitspaket liefert die Grundlage für die Integration von Daten aus Labor (Labor-Datenbank), Hygiene (HyBase) und dem Klinischen Informationssystem (KIS) und den Ergebnissen der schnellen Labordiagnostik (AP1).
Das Arbeitspaket definiert ein interoperables Datenmodell und entwickelt auf der Basis dieses Modells ein semantisches Warehouse, in das Daten in regelmäßigen Abständen integriert werden können. Dieses semantische Warehouse ist die Basis für die Arbeiten in AP3, AP4 und AP5.
Das Warehouse ist in dem Sinne semantisch, dass es auf Interoperabilität achtet und Daten semantisch beschreibt und über Primärquellen hinweg verknüpft. Für die Speicherung und Integration von Daten wird ein Semantisches Warehouse aufgebaut, das auf sog. Wissensgraphen als Datenmodell aufbaut. Wissensgraphen sind eine Technologie, die mittlerweile von Playern wie Google, Amazon, Microsoft oder Facebook zur Modellierung von Daten und Wissen verwendet wird, um Daten semantisch zu beschreiben.
Bei der Entwicklung des Wissensgraphen werden existierende Vokabulare wiederverwendet, um klinische Daten zu beschreiben, wie z.B. die Human Phenotype Ontology, UMLS, SNOMED-CT, Foundational Model of Anatomy (FMA), Gene Ontology, Ontology of Clinical Research, etc.
Bei der Entwicklung des Datenmodells orientieren wir uns an den HL7-FHIR-Profilen sowie an dem im Rahmen der Medizininformatik-Initiative entwickelten Kerndatensatz.

Es wird ein Ansatz entwickelt, der ein verteiltes Data Warehouse realisiert, siehe Abbildung. Das Data Warehouse ist aufgeteilt in eine Klinik-spezifische Komponente, sowie eine zentrale Komponente (Collaboration Zone). Die Klinik-spezifische Komponente ist nochmals unterteilt in eine Healthcare Zone, in der sich die IT-Systeme der Krankenversorgung befinden, und eine hinreichend entkoppelte Research Zone. Die Extraktion und Qualitätssicherung der Daten aus den Primärsystemen erfolgt in der Healthcare Zone.
Nach Anonymisierung bzw. Pseudonymisierung und ggf. weiterer Aufbereitung gelangen die Daten auf die Server in der Research Zone des jeweiligen Krankenhauses. Dort werden die in AP3 entwickelten Modelle trainiert und abgelegt. Damit verlassen klinische Daten nicht die Krankenhäuser.
In den Research Zonen werden die Daten über Primärquellen integriert und in einem über die Kliniken hinweg einheitlichen Datenmodell abgelegt. Das ermöglicht klinikübergreifende Auswertungen und Abfragen für das KINBIOTICS Projekt.
Die maschinell gelernten Modell werden dezentral und lokal in den verschiedenen Research Zones trainiert; die Modelle werden über Instanzen hinweg trainiert und geteilt während die Daten nie die eigene Research Zone verlassen.
Der zweite Bestandteil des verteilten Data Warehouses ist die sog. Collaboration Zone. In der Collaboration Zone werden hygienische Daten aus den drei beteiligten Kliniken aggregiert. Diese Daten sind komplett anonymisiert und haben keinerlei Patient*innenbezug. Sie dienen als Basis zur Entwicklung des Observatoriums in AP4.
Die Wirksamkeit einer Antibiotikatherapie wird durch eine Vielzahl von Parametern beeinflusst: von patient*innenspezifischen klinischen Werten über molekularbiologische Zustände bis hin zu Einflüssen der Krankenhausumgebung.
Behandelnde Ärzt*innen verwenden diese Parameter bei der Wahl einer Antibiotikagabe, gestützt auf Leitlinien, medizinischem Wissen und Erfahrung. Das Zusammenwirken aller Faktoren ist jedoch bislang unbekannt und aufgrund der erwarteten Komplexität nur mit fortgeschrittenen Methoden der künstlichen Intelligenz zu entschlüsseln.
Dieses Arbeitspaket verfolgt die Entwicklung entsprechender Modelle zur KI-basierten Entscheidungsunterstützung bei der Wahl einer Antibiotikatherapie. Dazu betrachten wir drei Ziele bzgl. der Wirksamkeit eines Antibiotikums: maximale Effizienz (Erreger werden abgetötet), maximale Zielgerichtetheit (dadurch Eindämmung von Resistenzentwicklungen) und Minimierung von Nebenwirkungen.
Entscheidend bei der Wahl der Verfahren ist die Nachvollziehbarkeit des Zustandekommens und die Möglichkeit der Unsicherheitsquantifizierung einer Prognose: Ein KI-System kann Mediziner*innen in ihren Entscheidungen unterstützen, aber nicht ersetzen. Aus diesem Grund wird der Transparenz von Vorhersagen großes Gewicht beigemessen; Mediziner*innen sollen im Sinne der erklärbaren KI (“explainable AI”) erfahren, welche Faktoren maßgeblich zu konkreten Empfehlungen beitragen.
Zusammengefasst erlauben die beschriebenen Techniken eine computergestützte individualisierte Einschätzung der Wahrscheinlichkeit eines Therapieerfolgs und des Risikos des Auftretens einer Antibiotikaresistenz. Sie sind damit ein wichtiger Schritt in Richtung personalisierter Medizin. AP5 stellt sicher, dass behandelnde Ärzt*innen die Risikoprognosen ohne technische Hürden verwenden können.
In diesem Arbeitspaket wird ein datengetriebenes Erreger- und Resistenz-Observatorium entwickelt, das die Verbreitung und Häufung von Resistenzen simuliert, modelliert und visualisiert und damit Fragen nach dem Ursprung und der Verbreitung von Resistenzen sowie Korrelation mit anderen Variablen erlaubt.
Realisiert wird das Observatorium als sogenannter Digitaler Zwilling. Ein Digitaler Zwilling ist ein digitales Modell eines materiellen oder immateriellen Objektes oder Prozesses aus der realen Welt. Der Digitale Zwilling basiert auf aggregierten Daten aus dem Bereich Hygiene, die aus den HyBase Systemen der drei beteiligten Krankenhäuser extrahiert werden, zusätzlich zu semantischen Informationen zur Verschreibung von Antibiotika, geographischen und zeitlichen Metadaten, sowie Daten, die das Umfeld beschreiben (Nähe zu ländlichen Regionen, Wohnort von Patient*innen, die den Erreger trugen etc.).
Auf dieser Basis werden als Teil des Observatoriums Visualisierungen und Dashboards in Realzeit aktualisiert, die Auskunft über folgende Aspekte erlaubt:
-
In welchen Regionen Bielefelds gibt es Häufungen von bestimmten Erregern?
-
In welchen Bereichen der Kliniken treten Häufungen von Erregern auf?
-
Wie verbreiten sich Erreger innerhalb der Kliniken?
-
An welchen Stellen kommen neue Erreger in den Umlauf?
-
Welche Korrelationen gibt es zwischen der Häufung bestimmter Erreger und anderen Variablen (Verschreibung von Antibiotika, Geographie, Jahreszeit, Umweltfaktoren)
Im öffentlich zugänglichen Teil des Observatoriums sind Daten auf Makrobene und Trends sowie Korrelationen visualisiert und über einzelne Kliniken derart abstrahiert, damit kein Bezug zu einzelnen Kliniken oder gar Bereichen in den Kliniken selbst dargestellt werden kann.
Dieses Modell soll bei der Suche nach Ursachen für die Verbreitung von Resistenzen unterstützen und damit der Entwicklung von Strategien zur Eindämmung von Resistenzen dienen. Darüber hinaus unterstützt es auch bei der ambulanten Therapierung zu Vergabe spezifischer Antibiotika unter Berücksichtigung der lokalen Erregerstatistiken im Sinne der S3-Leitlinie.
Somit ist das Observatorium als ein Teil des zu entwickelnden Entscheidungsunterstützungssystems zu sehen; durch das Observatorium können Ärzt*innen einen Überblick über die Verbreitung von Erregern und von Resistenzen erlangen und diese allgemein bei ihren Verschreibungspraktiken berücksichtigen. Im Rahmen dieses Arbeitspaketes wird das Observatorium evaluiert in Form von Umfragen mit Medizinern aus der Praxis aus dem Raum Bielefeld.
Ziel dieses Arbeitspaketes ist zum einen die Entwicklung eines funktionierenden Piloten des Expert*innensystems zur Unterstützung von Mediziner*innen bei der Diagnose und Wahl eines geeigneten Antibiotikums.
Das Design des Expert*innensystems richtet sich nach der S3-Linie und Integriert Entscheidungsunterstützung bei der Erstkalkulation einer Therapie, sowie bei der Re-Evaluierung und ggf. Vergabe eines zielgenauen Antibiotikums. Das Modell zur Vorhersage der Wirksamkeit bzw. Unwirksamkeit eines Antibiotikums aus AP3 ist integraler Bestandteil des Expert*innensystems.
Der Pilot wird realisiert in Form einer Web-Applikation, die in einem ersten Schritt im Hinblick auf Nutzbarkeit entwickelt und getestet wird. Für die Entwicklung der Applikation werden zunächst Papier-Prototypen entwickelt, die potentiellen zukünftigen Nutzer*innen vorgelegt werden. Nach erfolgreicher Validierung der Konzepte wird der Prototyp als Web-Applikation umgesetzt. Die Nutzbarkeit wird mit Standard-Werkzeugen der Evaluierung im Bereich der Softwareentwicklung sichergestellt, insbesondere mit dem SUS Test. Die Usability-Evaluation berücksichtigt insbesondere den Zugang zur Software für Menschen mit Beeinträchtigungen und stellt die Barrierefreiheit des entwickelten Piloten sicher. Hier kommen Prinzipien des Universal Design zur Anwendung.
Jenseits der Nutzbarkeit soll in diesem Paket die Güte der Vorhersagen des prädiktiven Systems systematisch evaluiert werden, um die Unbedenklichkeit einer praktischen Anwendung des Tools sicherzustellen und damit die Grundlage für eine spätere Erprobung unter realen Versorgungsbedingungen zu schaffen. Dabei soll mit Hilfe des Piloten die Validität der abgegebenen Antibioseempfehlungen im Hinblick auf den Therapieerfolg untersucht werden.
Die Evaluation erfolgt retrospektiv auf Grundlage von Patient*innenfällen, die nicht für das Training der KI herangezogen wurden. Analog zur Operationalisierung des Therapieerfolgs im Rahmen der Modellentwicklung (AP3) wird für die beobachteten Testfälle festgelegt, ob eine getätigte Antibiotikagabe zu einem gewünschten Ergebnis geführt hat oder nicht. Die erklärenden Patient*innenparameter der Testfälle werden dann in das Prognosetool gegeben, welches Erfolgswahrscheinlichkeiten für verschiedene Antibiotikatypen ermittelt. Die Ergebnisse der Toolberechnungen werden dann mit den in den Testdaten beobachtbaren Antibiotikagaben vor dem Hintergrund des damit assoziierten Therapieerfolgs verglichen und anhand von zuvor zu definierenden Fehlertoleranzniveaus bewertet. Dabei ist geplant, auch die Auswirkungen einer Nicht-Verfügbarkeit einzelner Datenmodalitäten bezüglich der Güte der Prognosen in den Blick zu nehmen und den (ökonomischen) Mehrwert zusätzlich erhobener Daten anhand von Simulationen zu untersuchen.
Da die Umsetzung der beschriebenen Evaluation im Wesentlichen von der konkreten Ausgestaltung des prognostischen Modells abhängt, erfolgt die Planung der Evaluation in enger Zusammenarbeit mit der Modellentwicklung (AP3). Alle Auswertungen erfolgen unter besonderer Berücksichtigung möglicher Geschlechterunterschiede.
Insgesamt leistet die Evaluation einen Beitrag zur weiteren Feinjustierung des Prognosetools und schafft die Voraussetzungen für eine perspektivische Implementierung in der Versorgungspraxis. So lassen sich etwa auf Grundlage der Analysen zur Datenverfügbarkeit kritische Datenmodalitäten identifizieren, die im Einzelfall zwingend bereitstehen müssen, um das Tool praktisch nutzen zu können.
Nach erfolgreicher Evaluation der Prognosen können die tatsächlichen Versorgungseffekte des Entscheidungsunterstützungstools im Rahmen einer prospektiv angelegten kontrollierten Studie an der*dem Patient*in abgesichert werden. Hierfür wird im Rahmen des Arbeitspakets ein Studien-/Evaluationskonzept entwickelt, welches im Sinne der Nachhaltigkeit der Projektergebnisse die Grundlage für ein entsprechendes Folgeprojekt bildet.
Im Rahmen von AP6 werden die organisationalen Implementationsbedingungen des KINBIOTICS-Systems analysiert und in Form eines Implementationsleitfadens in die praxisbezogene Translation überführt. Das Forschungsziel ist die Identifikation organisationaler und prozessualer Determinanten von fördernden und hemmenden Bedingungen der Nutzung der Technologie im klinischen Alltag.
Dabei wird untersucht, wie die Intervention in der Versorgungspraxis optimal unter Alltagsbedingungen implementiert werden kann, welche bisher nicht genauer untersuchten organisationalen und Kontextmerkmale die Effektivität beeinflussen und wie die Akzeptanz bei Leistungserbringer*innen durch die gezielte Veränderung personeller und struktureller Bedingungen in der stationären Versorgung optimiert werden kann. Hierdurch wird ein gelingender Innovations- und Nutzentransfer in die Versorgungspraxis gefördert und die Nachhaltigkeit und praktische Translation der Innovationsentwicklung unterstützt.
Den nachfolgenden Forschungsfragen und methodischen Teilschritten liegen die Definition intelligenter technischer Systeme als soziotechnische Innovationen und die damit verbundenen arbeitspraktischen, wertorientierten, ethischen und ökonomischen Wechselwirkungen zwischen Nutzer*innen (Ärzt*innen), Technologie (Algorithmen) und Organisation (stationäre Versorgung) zugrunde.
-
Welche fördernden und hemmenden Implementationsbedingungen des KINBIOTICS- Systems in der stationären Versorgung können unter Berücksichtigung und Bewertung der Übertragbarkeit von internationalen Forschungsergebnissen identifiziert werden?
-
Welche organisationalen Bedingungen und Kontextvariablen determinieren den Prozess der Implementierung des KINBIOTICS-Systems in der stationären Versorgung?
-
Nach welchen strukturellen Merkmalen der stationären Versorgung (z.B. Versorgungszone und -stufe, Bettenzahl, Region, Einzugsgebiet, Entwicklungsstand der Krankenhaus-IT) unterscheiden sich die identifizierten Implementationsdeterminanten?
-
Welche personellen, strukturellen und kulturellen Bedingungen müssen in der stationären Versorgung vorhanden sein, um den Innovationstransfer des KINBIOTICS-Systems zu fördern, und wie können diese priorisiert werden?
Für die Analyse wird auf einen Mixed-Method-Ansatz zurückgegriffen, der literaturbasierte, qualitative und quantitative Elemente der empirischen Implementationsforschung aufeinander aufbauend integriert:
-
Systematisches Review (Fragestellung 1),
-
Problemzentrierte Einzelinterviews (operative Ebene Leistungserbringer*innen und Hygieneverantwortliche; Bezug: der der Leistungserbringer*innen, ökonomischen regional in den Leitung, beteiligten Leitungsebene der Qualitätsmanagement, Modellkliniken,
n_max=15) (Fragestellung 2 und 4), -
Onlinebasiertes Expert*innenpanel (Leitungsebene der Leistungserbringer*innen und der ökonomischen Leitung, Qualitätsmanagement, Hygieneverantwortliche; Bezug: deutschlandweit,
n_max=100) (Fragestellung 3 und 4).
Aus den erfassten Ergebnissen wird der Implementationsleitfaden entwickelt.
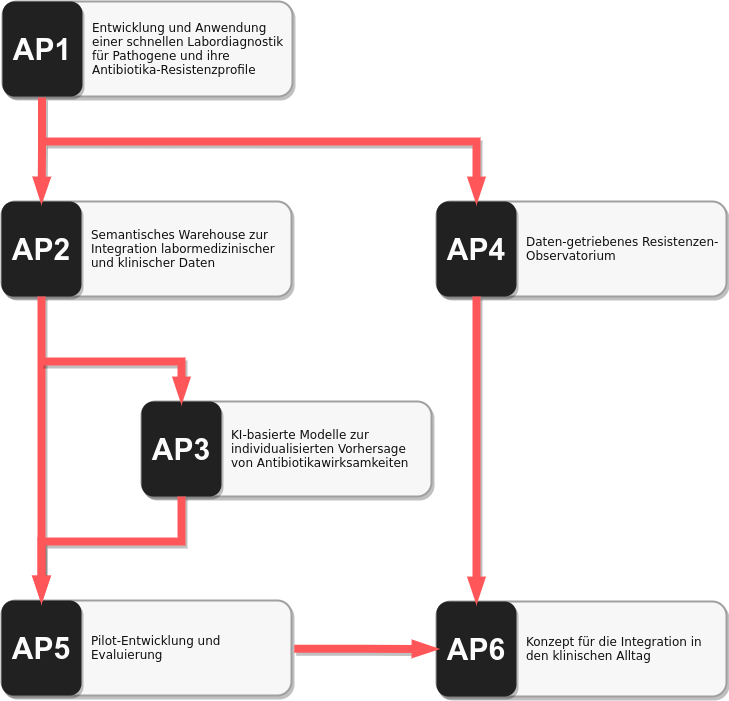
Die Abhängigkeiten der Arbeitspakete ergeben sich aus folgendem Diagramm: